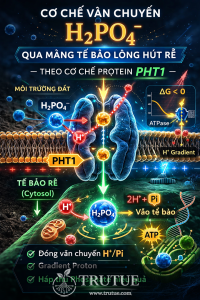
Vai trò của protein AMT1 và nền tảng nhiệt động học
1. Khái quát
Nitơ là nguyên tố khoáng thiết yếu đối với thực vật, tham gia cấu tạo axit amin, protein, axit nucleic và nhiều phân tử sinh học quan trọng khác. Trong môi trường đất, nitơ vô cơ tồn tại chủ yếu dưới hai dạng: nitrate (NO₃⁻) và ammonium (NH₄⁺).
Ở nhiều hệ sinh thái như đất ngập nước, đất chua hoặc môi trường có hoạt động vi sinh vật mạnh, NH₄⁺ có thể chiếm ưu thế. Tuy nhiên, do mang điện tích dương, NH₄⁺ không thể khuếch tán tự do qua lớp lipid kép của màng sinh chất. Vì vậy, sự hấp thu ammonium phụ thuộc vào các protein vận chuyển chuyên biệt nằm trên màng tế bào rễ.
Nhóm protein AMT (Ammonium Transporter), đặc biệt là AMT1, đóng vai trò trung tâm trong quá trình này.
2. Cơ sở nhiệt động học của vận chuyển NH₄⁺
Sự di chuyển của ion qua màng sinh học chịu chi phối bởi gradient điện hóa, bao gồm:
-
Chênh lệch nồng độ
-
Chênh lệch điện thế màng
Năng lượng tự do Gibbs (ΔG) của quá trình vận chuyển được biểu diễn theo phương trình:
ΔG=RTln(CinCout)+zFψΔG = RT \ln \left(\frac{C_{in}}{C_{out}}\right) + zFψ
Trong đó:
-
R: hằng số khí
-
T: nhiệt độ tuyệt đối
-
C_in: nồng độ nội bào
-
C_out: nồng độ ngoại bào
-
z: điện tích ion (z = +1 đối với NH₄⁺)
-
F: hằng số Faraday
-
ψ: điện thế màng
2.1 Thành phần hóa học
Biểu thức:
RTln(Cin/Cout)RT \ln(C_{in}/C_{out})
phản ánh xu hướng ion di chuyển theo gradient nồng độ. Nếu nồng độ bên ngoài cao hơn bên trong, thành phần này mang giá trị âm và quá trình vận chuyển trở nên thuận lợi về mặt hóa học.
2.2 Thành phần điện học
Thành phần:
zFψzFψ
phản ánh ảnh hưởng của điện thế màng. Ở tế bào rễ, điện thế màng thường âm (khoảng −120 đến −200 mV). Vì NH₄⁺ mang điện tích dương, điện thế âm sẽ tạo lực hút, làm tăng khả năng ion đi vào tế bào.
2.3 Ý nghĩa của ΔG
-
ΔG < 0: vận chuyển thuận lợi
-
ΔG = 0: cân bằng điện hóa
-
ΔG > 0: không tự phát
Do đó, quá trình hấp thu NH₄⁺ phụ thuộc trực tiếp vào trạng thái điện hóa của màng tế bào.
3. Protein AMT1 và cơ chế mở luân phiên (Alternating-Access)
AMT1 không hoạt động như một kênh mở liên tục xuyên qua màng. Thay vào đó, protein này vận hành theo cơ chế gọi là alternating-access (mở luân phiên).
Nguyên tắc cơ bản của cơ chế này là:
Protein không bao giờ mở đồng thời về cả hai phía của màng. Thay vào đó, nó thay đổi cấu hình để lần lượt mở ra phía ngoài và phía trong.
Cơ chế này đảm bảo:
-
Tính chọn lọc cao
-
Ngăn rò rỉ ion
-
Kiểm soát hướng vận chuyển
4. Các trạng thái cấu hình của AMT1
Quá trình vận chuyển NH₄⁺ có thể được chia thành ba trạng thái cấu trúc chính.
4.1 Trạng thái E1 – Mở ra ngoài
Ở trạng thái này, vị trí gắn của protein hướng về phía môi trường đất. NH₄⁺ từ ngoại bào tiếp cận và gắn vào vị trí đặc hiệu trên protein.
Xác suất gắn phụ thuộc vào:
-
Nồng độ NH₄⁺ bên ngoài
-
Điện thế màng
Khi nồng độ ngoại bào tăng, khả năng gắn ion tăng tương ứng.
4.2 Trạng thái Occluded – Đóng kín
Sau khi ion gắn vào, protein thay đổi cấu hình và đóng kín cả hai phía, giữ ion trong một khoang nội tại.
Trạng thái này:
-
Ngăn sự rò rỉ ngược
-
Chuẩn bị cho quá trình chuyển cấu hình
Trong môi trường kỵ nước bên trong protein, có khả năng xảy ra quá trình khử proton:
NH₄⁺ → NH₃ + H⁺
Do NH₃ trung tính dễ di chuyển hơn trong môi trường ít phân cực. Đây là một giả thuyết được đề xuất dựa trên đặc điểm cấu trúc của họ protein AMT/Mep/Rh.
4.3 Trạng thái E2 – Mở vào trong
Protein tiếp tục thay đổi cấu hình và mở về phía bào tương.
Ion (hoặc NH₃) được giải phóng vào môi trường nội bào. Ở pH sinh lý (~7.2), dạng ammonium proton hóa (NH₄⁺) chiếm ưu thế, do đó phân tử có xu hướng tồn tại ở dạng tích điện trong tế bào.
Sau khi giải phóng cơ chất, protein trở về trạng thái ban đầu (E1) và chu trình lặp lại.
5. Vai trò của điện thế màng
Điện thế màng được duy trì chủ yếu nhờ hoạt động của bơm H⁺-ATPase, tạo ra sự chênh lệch điện tích giữa hai phía màng.
Điện thế âm bên trong tế bào:
-
Làm giảm ΔG của quá trình
-
Tăng xác suất vận chuyển cation
-
Đóng vai trò nguồn năng lượng gián tiếp
Do đó, hấp thu NH₄⁺ không chỉ phụ thuộc vào nồng độ mà còn phụ thuộc mạnh vào trạng thái điện sinh lý của tế bào.
6. Động học và điều hòa
Tốc độ vận chuyển NH₄⁺ tăng theo nồng độ ngoại bào đến một mức bão hòa, phản ánh đặc điểm động học phụ thuộc cơ chất của protein vận chuyển.
Tuy nhiên, sự tích lũy ammonium quá mức có thể gây:
-
Rối loạn pH nội bào
-
Ức chế sinh trưởng
-
Mất cân bằng chuyển hóa carbon – nitơ
Do đó, hoạt động của AMT1 được điều hòa chặt chẽ ở mức phiên mã và hậu dịch mã.
7. Vì sao AMT1 không phải là một kênh ion?
Nếu protein tạo lỗ mở liên tục:
-
Ion có thể khuếch tán hai chiều tự do
-
Điện thế màng sẽ suy giảm
-
Kiểm soát nội môi bị phá vỡ
Cơ chế alternating-access ngăn điều này bằng cách đảm bảo rằng khoang gắn không bao giờ đồng thời tiếp xúc với cả hai phía.
Điểm khác biệt này là nền tảng phân biệt transporter và channel ở cấp độ phân tử.
8. Hệ quả sinh lý
Hấp thu NH₄⁺ mang lại lợi thế năng lượng so với nitrate vì không cần quá trình khử trước khi đồng hóa vào glutamine.
Tuy nhiên, ammonium dư thừa có thể gây độc tính. Do đó, AMT1 được điều hòa ở nhiều mức:
-
Điều hòa biểu hiện gen
-
Điều hòa thông qua phosphoryl hóa
-
Điều chỉnh theo trạng thái dinh dưỡng của cây
9. Kết luận
Vận chuyển NH₄⁺ qua màng tế bào rễ là kết quả của:
-
Gradient điện hóa
-
Biến đổi cấu hình protein
-
Phân bố xác suất nhiệt động học
AMT1 hoạt động như một transporter điển hình theo cơ chế alternating-access, trong đó sự thay đổi cấu trúc đóng vai trò trung tâm.
Ở cấp độ phân tử, đây không phải là quá trình cơ học đơn giản mà là một hệ thống cân bằng năng lượng được điều hướng bởi cấu trúc protein và điều kiện điện hóa của tế bào.